Tratamiento de un hurón (Mustela putorius furo) con coronavirus sistémico (FSCV) mediante el análogo de nucleósidos GS-441524 subcutáneo
Nucleoside analogue GS-441524 subcutaneous treatment of a ferret (Mustela putorius furo) with systemic coronavirus (FSCV)
A. Riera, N. Morera, I. Díaz, A. Serra, A. Calvo
Contacto: rieraroca@hotmail.com
Resumen
La enfermedad causada por el coronavirus sistémico del hurón (Ferret Systemic Coronavirus Disease, FSCVD) resulta letal en la mayoría de los casos. No se ha descrito ningún tratamiento efectivo y la mayoría de los hurones afectados mueren o terminan siendo eutanasiados debido a la evolución de la enfermedad. El GS-441524 se ha utilizado de manera efectiva para el tratamiento de la peritonitis infecciosa felina (PIF) en gatos, enfermedad similar a la FSCVD. Un hurón con enfermedad por coronavirus sistémico ha sido tratado con un producto sin licencia que contiene GS-441524, por vía subcutánea, durante 12 semanas, consiguiendo la remisión total de la enfermedad. Según nuestro conocimiento, el tratamiento completo vía subcutánea con GS-441524 en un hurón enfermo por FSCVD, sin la transición al tratamiento oral, no ha sido descrito anteriormente.
Palabras clave: GS-441524, remdesivir, coronavirus sistémico, hurones.
Clin Vet Peq Anim 2025, 45 (3): 187-191
Summary
Ferret Systemic Coronavirus Disease (FSCVD) is lethal in most cases. Until now there has been no effective treatment and many of the affected ferrets die or are euthanized because of the disease. GS-441524 is used effectively in the treatment of cats with feline infectious peritonitis (FIP), which is similar to FSCVD. A ferret with FSCVD has been treated with an unlicensed product that contains GS-441524, subcutaneously, for 12 weeks. Complete remission of the disease has been achieved. To our knowledge, complete subcutaneous treatment of GS-441524 in a ferret with FSCVD, without transition to an oral treatment, has not been previously reported.
Keywords: GS-441524, remdesivir, systemic coronavirus, ferrets.
Clin Vet Peq Anim 2025, 45 (3): 187-191

La presencia de este logo en un artículo de la revista indica que se publicará un examen sobre el mismo en la plataforma AVEPA Elearning. Su resolución aporta 0,15 créditos dentro del sistema de acreditaciones de especialidades veterinarias de AVEPA.
Introducción
El coronavirus sistémico del hurón (FSCV) es el agente causal de una enfermedad piogranulomatosa sistémica, parecida a la forma seca de PIF en gatos, que afecta a los hurones con una alta tasa de mortalidad.1,2 Hasta ahora no se ha descrito ningún tratamiento efectivo.1 El análogo de nucleósidos GS-441524 es el metabolito activo del remdesivir, que ha demostrado su eficacia y seguridad en el tratamiento de emergencia de COVID-19 en humanos,3 de PIF en gatos4 y de SARS-CoV-2 en hurones.5 Debido a las similitudes entre las enfermedades PIF y la FSCVD, el análogo de nucleósidos GS-441524 puede ser una opción terapéutica eficaz para hurones que padezcan FSCV.
Este medicamento no se encuentra aprobado para su uso en veterinaria en nuestro país ni en muchos otros. En países como Reino Unido y Australia existen antivirales (remdesivir y GS-441524) formulados legalmente para su uso en gatos.6 El objetivo del presente trabajo es describir, mediante un caso clínico, la utilidad del GS-441524 por vía subcutánea (SC) para el tratamiento de la FSCVD.
Caso clínico
Un hurón macho no castrado, de 2 años y 1,45 kg de peso, mantenido con una dieta de pienso extrusionado para hurón, acudió a consulta por un cuadro de apatía, anorexia, temblores, debilidad del tercio posterior y una crisis convulsiva. Durante la exploración física se observó que estaba alerta, con temblores, mucosas ligeramente pálidas y dolor a la palpación abdominal. Se palparon diferentes masas en abdomen caudal. El examen neurológico resultó dentro de la normalidad.
Se le realizó una analítica sanguínea en la que destacaba leucocitosis, neutrofilia e hiperproteinemia con hiperglobulinemia. Otros parámetros sanguíneos del hemograma y bioquímicos resultaron con valores dentro de la normalidad (Tabla 1).7
En negrita aparecen los valores fuera de los intervalos de referencia. MCV: volumen corpuscular medio; MCH: hemoglobina corpuscular media; MCHC: concentración de hemoglobina corpuscular media; ALT: alanina aminotransferasa; Bilir total: bilirrubina total; BUN: nitrógeno ureico sanguíneo; CA: calcio; FOS: fósforo; CREA: creatinina; GLU: glucosa; Na(+): sodio; K(+): potasio; GLOB: globulinas.
En la ecografía abdominal se observó esplenomegalia con parénquima heterogéneo, linfadenopatía abdominal generalizada y una masa hipoecoica de 2,6 cm de diámetro en la zona de proyección de los linfonodos mesentéricos (Fig. 1). También se observaron hallazgos ecográficos compatibles con peritonitis, como aumento de la ecogenicidad difusa del peritoneo y presencia de líquido libre anecoico, en este caso no puncionable. Por cuestiones económicas los tutores rechazaron ampliar los análisis sanguíneos con un proteinograma.
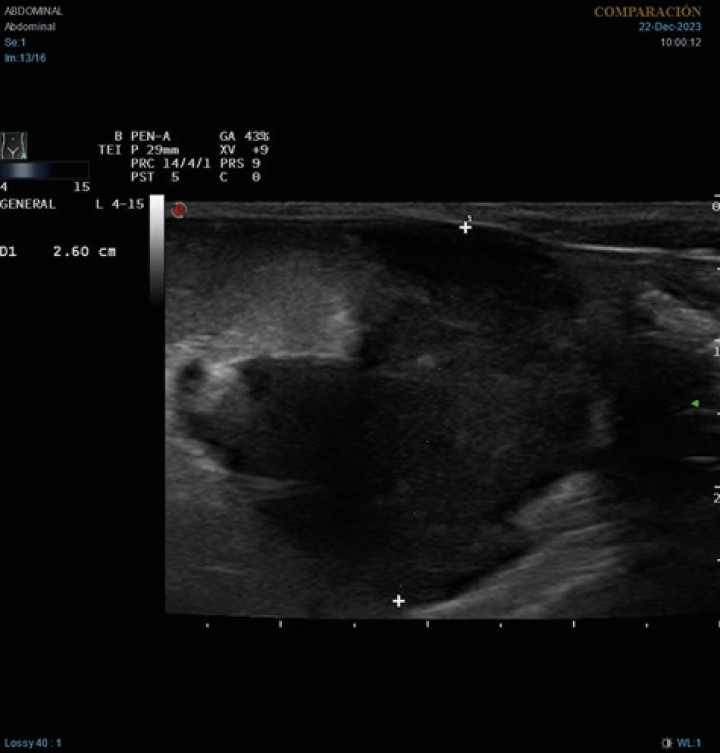
Figura 1
Imagen ecográfica longitudinal del abdomen caudal. Masa heterogénea, principalmente hipoecoica, de 2,6 cm de diámetro, con hiperecogenicidad de la grasa adyacente.
Se hospitalizó el paciente con un tratamiento inicial de amoxicilina-clavulánico (22 mg/kg/12 h/IV Amoxicilina/Ácido clavulánico Normon 1000 mg/200 mg inyectable, Normon, Madrid, España), maropitant (1 mg/kg/24 h/IV, Prevomax Dechra, Uldum, Dinamarca) y fluidoterapia (Lactato de Ringer). Para el tratamiento del dolor se le administró en infusión continua ketamina (1 mg/kg/h Ketamidor VetViva, Wells, Austria) y fentanilo (2 µg/kg/h Fentadon Dechra, Uldum, Dinamarca). Durante el ingreso y la hospitalización el paciente no volvió a exhibir ninguna crisis convulsiva.
Bajo sedación con butorfanol (0,1 mg/kg IV Torphasol, aniMedica Senden-Bösensell, Alemania) y alfaxolona (5 mg/kg IV, Alfaxan Dechra, Uldum, Dinamarca) se le realizó una punción con aguja fina ecoguiada de bazo y linfonodo mesentérico caudal. La citología fue compatible con inflamación piogranulomatosa, sin observarse una causa subyacente.
El día siguiente se tomaron muestras de biopsia mediante una laparotomía exploratoria. Tras la sedación preanestésica con butorfanol y la inducción anestésica con alfaxolona a las mismas dosis anteriormente indicadas, el paciente se intubó con un tubo de 2,5 de diámetro con manguito y se mantuvo con sevofluorano al 2-3 % (SevoFlo 100 %, Zoetis Louvain-La-Neuve, Bélgica) con oxígeno al 100 % en un circuito abierto (T de Ayre) y respiración espontánea. En la exploración abdominal mediante laparotomía media, se observaron los linfonodos mesentérico caudal, sublumbar e ilíacos pálidos y de aspecto granuloso. Se tomaron muestras de estos linfonodos para histopatología y cultivo. Se realizaron lavados y aspiración de la cavidad abdominal con solución salina y se cerró por planos de forma rutinaria. El paciente se recuperó de manera satisfactoria.
El estudio histopatológico mostró una linfadenitis piogranulomatosa grave y generalizada; la totalidad de los fragmentos evaluados estaban ocupados por múltiples piogranulomas compuestos por centros de tejido necrótico y neutrófilos degenerados rodeados por abundantes macrófagos, células linfoplasmocitarias y fibroblastos reactivos. No se visualizaron microorganismos. La muestra fue positiva al RT-PCR (Real Time Polymerase Chain Reaction) del coronavirus entérico del hurón (FECV). El cultivo microbiológico resultó negativo. El diagnóstico de enfermedad por coronavirus sistémico del hurón (FSCVD) se confirmó mediante el análisis inmunohistoquímico frente al coronavirus felino del linfonodo mesentérico remitido. El anticuerpo utilizado presentaba positividad cruzada con el FSCV (Idexx laboratorios, Barcelona, España) (Fig. 2).
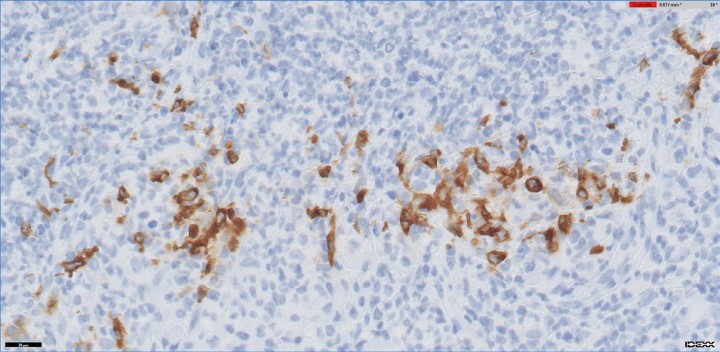
Figura 2
Imagen histológica del linfonodo mesentérico 60 x. Tinción inmunohistoquímica. Numerosos macrófagos presentan inmunopositividad frente al anticuerpo con positividad cruzada con el coronavirus sistémico del hurón. Imagen cortesía de Laboratorios IDEXX.
El paciente fue dado de alta con un tratamiento de prednisona (1 mg/kg q 12 h PO, Estilsona gotas orales, Laboratorios Ern, Barcelona, España) y famotidina (0,5 mg/kg q 24 h PO, Famotidina Cinfa 20 mg, Huarte, España), durante una semana.
Los tutores se pusieron en contacto con la página web CureFIP.com y trataron al hurón con GS-441524 (8 mg/kg cada 24 h SC, Cure FIP20) durante 12 semanas, según protocolo indicado por los responsables de la página web para el tratamiento de la PIF en gatos.
Durante el tratamiento el hurón presentó en dos ocasiones reacciones en el lugar de la inyección, caracterizadas por vesículas y fístulas (Fig. 3A). Estas lesiones se resolvieron con el rasurado de la zona, lavados con solución salina fisiológica estéril y la aplicación de una solución tópica de ácidos grasos hiperoxigenados (Mepentol Alfasigma, Barcelona, España) (Fig. 3B).
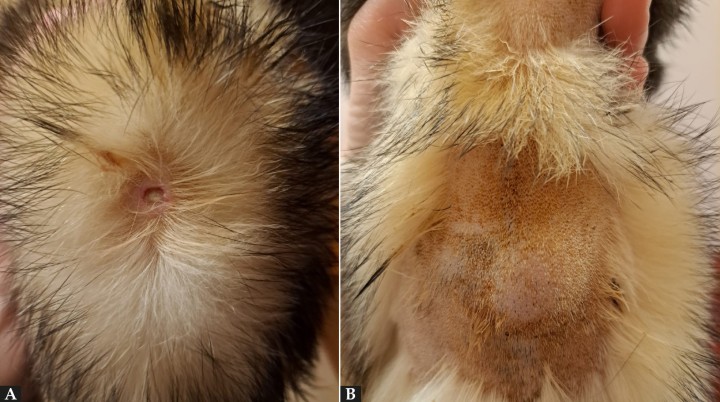
Figura 3
(A) Imagen del dorso del paciente. Lesión cutánea ulcerativa en la zona de administración SC. (B) Imagen de la misma zona tras el tratamiento tópico.
A los 15 días de iniciarse el tratamiento con GS-441524 desaparecieron los síntomas iniciales. La exploración física general resultó correcta, la palpación abdominal no dolorosa y la ecografía abdominal mostró una clara disminución del tamaño de los linfonodos abdominales caudales. Las proteínas totales se mantuvieron elevadas (Tabla 1). A los 15 días de finalizar el tratamiento (16 semanas tras la presentación) se realizó otro control con exploración física general, ecografía abdominal y analítica sanguínea con resultados dentro de la normalidad. La concentración de las proteínas séricas totales y las globulinas disminuyeron hasta valores normales (Tabla 1). Seis meses después del alta el hurón sigue sin presentar signos clínicos de enfermedad.
Discusión
La FSCD es la enfermedad piogranulomatosa en hurones parecida a la forma seca de la PIF en gatos. Sin ningún tratamiento eficaz, esta enfermedad se considera letal. La terapia de inmunosupresión y de soporte ayudan a mantener en algunos casos cierta calidad de vida.1
En este artículo se describe el caso de un hurón diagnosticado con FSCVD, medicado con GS-441524 vía SC durante 12 semanas, de la misma manera que el tratamiento de PIF en gatos. El hurón exhibió una rápida mejora. Una publicación describe el tratamiento oral con GS-4411524 de tres hurones con FSCVD.8 La evolución de estos tres hurones y el nuestro es parecida, con una remisión rápida de los signos clínicos y una posterior normalización de la hiperproteinemia, tal como sucede también en gatos con PIF tratados con GS-4411524.9
Los tutores del hurón prefirieron la administración inyectable debido a la dificultad en administrar medicación por vía oral en su mascota. En gatos con PIF la administración de GS-4411524 parenteral u oral, o la transición de una a otra, parecen ser igualmente efectivas.9 Nuestro caso junto con los tres hurones con FSCVD tratados con GS-4411524 oral8 indicarían que en hurones puede suceder lo mismo.
Los únicos efectos adversos observados fueron lesiones cutáneas ulcerativas en la zona de administración, atribuidas al uso de medicación inyectable SC durante largo tiempo y al bajo pH del producto. El pH real de Cure PIF® inyectable es de 1,1-1,3, muy por debajo de un pH fisiológico.10 La patogénesis de las lesiones cutáneas inducidas por Cure PIF® vía SC en gatos parece ser de naturaleza química, por la acidez del producto, lo que provoca una reacción inflamatoria piogranulomatosa no infecciosa y cicatricial.11 En hurones parece suceder lo mismo; en nuestro caso estas heridas no fueron importantes y se solucionaron con el tratamiento tópico descrito.
Aunque no se observaron otras complicaciones, no pueden descartarse efectos adversos durante el tratamiento, ya que, por decisión de los tutores del hurón, el control analítico se compuso únicamente de un análisis del hematocrito y las proteínas séricas a los 15 días del tratamiento, y un análisis completo a los 15 días tras finalizarlo. Un control analítico más exhaustivo podría determinar si existen efectos secundarios durante el tratamiento SC con GS-4411524 en hurones.
El tratamiento inyectable vía SC con GS-441524 a la dosis de 8 mg/kg cada 24 h durante 12 semanas resolvió la sintomatología asociada a la infección por el virus de la FSCD en un hurón, observándose complicaciones menores en la piel. En casos en que sea difícil la administración oral de medicación, la administración de GS-441524 inyectable por vía subcutánea puede ser una alternativa válida para hurones con FSCD. Serían necesarios estudios que determinen la dosificación mínima efectiva, la duración del tratamiento y la toxicidad del GS-441524 en hurones.
Agradecimientos
Los autores quieren agradecer a Esther Torres su dedicación en este y muchos otros casos y a Alejandro López la ayuda con el manuscrito. Agradecimientos a Laboratorios Idexx por la cesión de la imagen histológica.
Fuente de financiación: Este trabajo no se realizó con fondos comerciales, públicos o del sector privado.
Conflicto de intereses: Los autores declaran que no existen conflictos de intereses.
Aclaración: Los autores clarifican que este fármaco fue usado fuera de la cascada de prescripción.
Bibliografía
- 1.
Hoefer H: Gastrointestinal Diseases of Ferrets. En: Quesenberry KE, Orcutt CJ, Mans C, Carpenter JW (eds): Ferrets, Rabbits, and Rodents Clinical Medicine and Surgery, Elsevier, 2022; 27-38.
- 2.
Garner MM, Ramsell K, Morera N, et al. Clinicopathologic Features of a Systemic Coronavirus-Associated Disease Resembling Feline Infectious Peritonitis in the Domestic Ferret (Mustela putorius). Veterinary Pathology 2008; 45(2): 236-246.
[PubMed] - 3.
Ison MG, Wolfe C, Boucher HW: Emergency use authorization of remdesivir: the need for a transparent distribution process. JAMA 2020; 323(23): 2365-2366.
[PubMed] - 4.
Pedersen NC, Perron M, Bannasch M et al. Efficacy and safety of the nucleoside analog GS-441524 for treatment of cats with naturally occurring feline infectious peritonitis. J Feline Med Surg 2019; 21(4): 271-281.
[PubMed] - 5.
Cox RM, Wolf JD, Lieber CM et al. Oral prodrug of remdesivir parent GS-441524 is efficacious against SARS-CoV-2 in ferrets. Nature Communications 2021; 12: 6415-6426.
[PubMed] - 6.
Taylor SS, Coggins S, Barker EN, et al. Retrospective study and outcome of 307 cats with feline infectious peritonitis treated with legally sourced veterinary compounded preparations of remdesivir and GS-441524 (2020–2022). J Feline Med Surg 2023; 25(9): 1098612X231194460.
[PubMed] - 7.
Quesenberry KE, de Matos R: Basic Approach to Veterinary Care of Ferrets. En Quesenberry KE, Orcutt CJ, Mans C, Carpenter JW (eds). Ferrets, Rabbits, and Rodents Clinical Medicine and Surgery. Elsevier, 2022; 13-26.
- 8.
Puffal J, Neece AJ, Scaletti F: Treatment of Three Ferrets Diagnosed with Ferret Systemic Coronaviral Disease Using the Nucleoside Analogue GS-441524. Animals (Basel) 2024; 14(6): 916.
[PubMed] - 9.
Coggins SJ, Norris JM, Malik R, et al. Outcomes of treatment of cats with feline infectious peritonitis using parenterally administered remdesivir, with or without transition to orally administered GS-441524. J Vet Intern Med 2023; 37(5): 1772-1783.
[PubMed] - 10.
Kent AM, Guan S, Jaque N et al: Unlicensed antiviral products used for the at-home treatment of feline infectious peritonitis contains GS-441524 at significantly different amounts than advertised. J Am Vet Med Assoc 2024; 262 (4): 489-497.
[PubMed] - 11.
Calvo A, Ramírez I, Frías I, Ordeix L: Características clínico-patológicas de la dermatitis nodular-ulcerativa asociada al punto de inóculo de un producto a base de GS-441524, administrado para el tratamiento de la peritonitis infecciosa felina. SEVC 2024, Madrid.