Caso clínico de… Urgencias
Contacto: italas@urgenciesveterinaries.com
Introducción
El acenocumarol (Sintrom) es un derivado de la cumarina que actúa como antagonista de la vitamina K inhibiendo la gamma carboxilación hepática de los factores de coagulación dependientes de la vitamina K.1 Se utiliza en medicina humana como tratamiento y profilaxis de las afecciones tromboembólicas.
La ingesta de este fármaco por parte de las mascotas que conviven con personas que se medican con acenocumarol puede, por lo tanto, provocar alteraciones en la coagulación del mismo modo que la ingesta de raticidas cumarínicos.2
No se describen casos de intoxicación por acenocumarol en veterinaria, y en humana solo se describe un caso de ingesta accidental en una niña de 20 meses de edad.3
Cada vez es más frecuente encontrar casos de intoxicación en animales por ingesta de medicamentos que utilizan las personas y es por esto también que es importante tener en cuenta estas posibles intoxicaciones con las que estamos menos familiarizados.
Presentamos dos casos de ingesta de acenocumarol y su manejo.
Historia
Se presentaron de urgencias dos pacientes. Las dos se habían quedado solas en casa y habían ingerido pastillas de SINTROM 4 mg comprimidos (acenocumarol. Merus Labs Luxco II S.À.R.L., Luxemburgo). No podían contabilizar cuántas habían ingerido, ni a qué hora. Las dos pacientes se encontraban hemodinámicamente estables, sin signos de hemorragia.
Caso 1
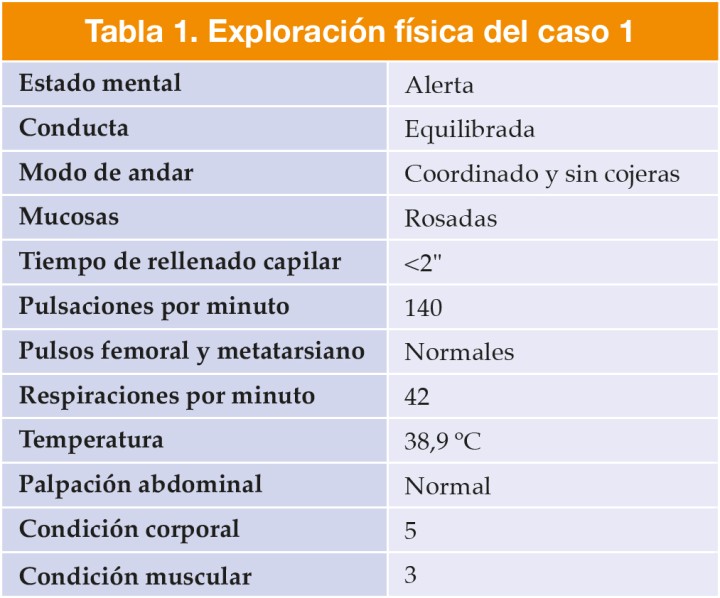
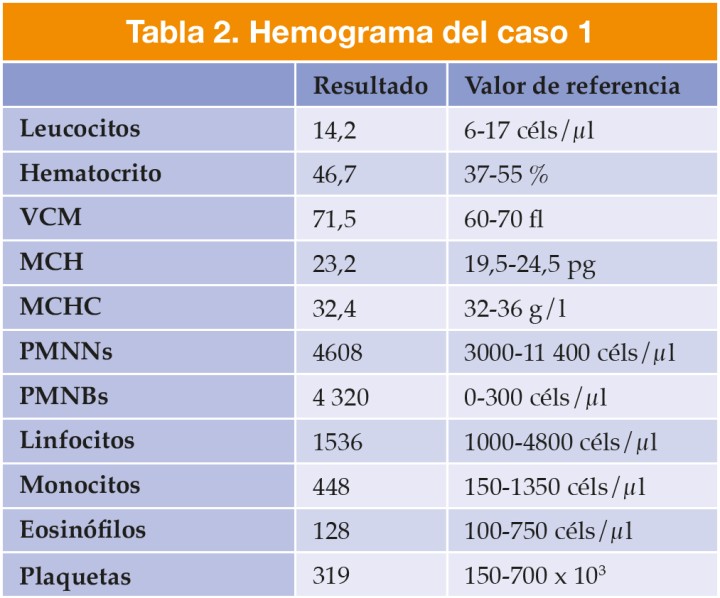
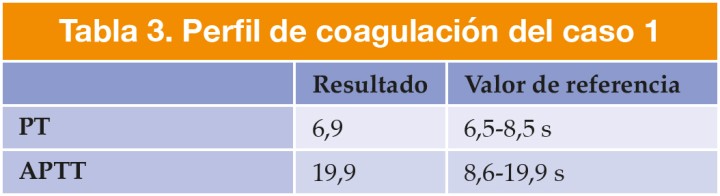
Se trataba de una perra hembra no castrada de raza pinscher enano, de 14 meses de edad y 1,8 kg de peso. Se realizó una exploración física y pruebas complementarias (Tablas 1, 2 y 3).
VCM: volumen corpuscular medio; MCH: hemoglobina corpuscular media; MCHC: concentración de hemoglobina corpuscular media; PMNNs: neutrófilos polimorfonucleares; PMNBs: basófilos polimorfonucleares.
PT: tiempo de protrombina; APTT: tiempo parcial de tromboplastina activada.
Como tratamiento, se administró apomorfina (Emedog 1 mg/ml, Dômes Pharma, Pont-du-Château) 0,1 mg/kg de forma subcutánea, para inducir el vómito. La paciente vomitó contenido gástrico, sin observarse la presencia de restos de pastillas. También se administró vitamina K1 endovenosa lenta (Vitamina K1 10 mg/ml, Dômes Pharma, Pont-du-Château), 5 mg/kg/12 horas. Se administró carbón activo con catártico (Carbodote Prime con carbón vegetal 30% y sulfato de sodio 6,25%, Dômes Pharma, Pont-du-Château), a dosis de 7,8 g, seguido de carbón activo solo (Carbodote Repeat con carbón vegetal 30%, Dômes Pharma, Pont-du-Château) a dosis de 7,2 g cada 6 horas.
La paciente no mostró síntomas relacionados con coagulopatía durante las horas que estuvo hospitalizada. Fue dada de alta a las 24 horas con tratamiento de vitamina K1 a dosis de 1 mg/kg vía oral, cada 12 horas, durante 3 semanas y con recomendación de monitorizar el tiempo de protrombina a las 48 y a las 72 horas después de acabar el tratamiento.
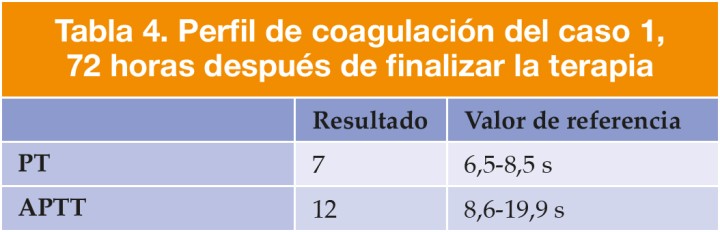
Los controles, realizados 72 horas después de finalizar el tratamiento con vitamina K1, dieron valores dentro de la normalidad (Tabla 4). No se realizaron controles a las 48 horas de finalizado el mismo.
PT: tiempo de protrombina; APTT: tiempo parcial de tromboplastina activada.
Caso 2
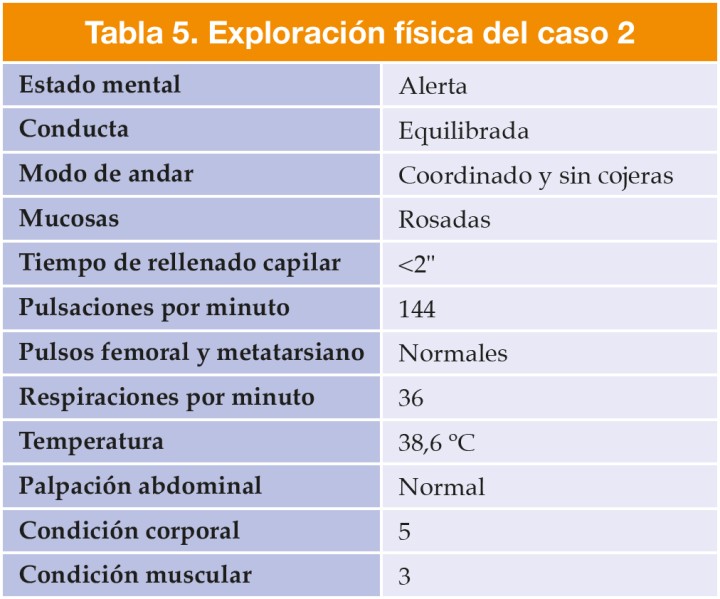
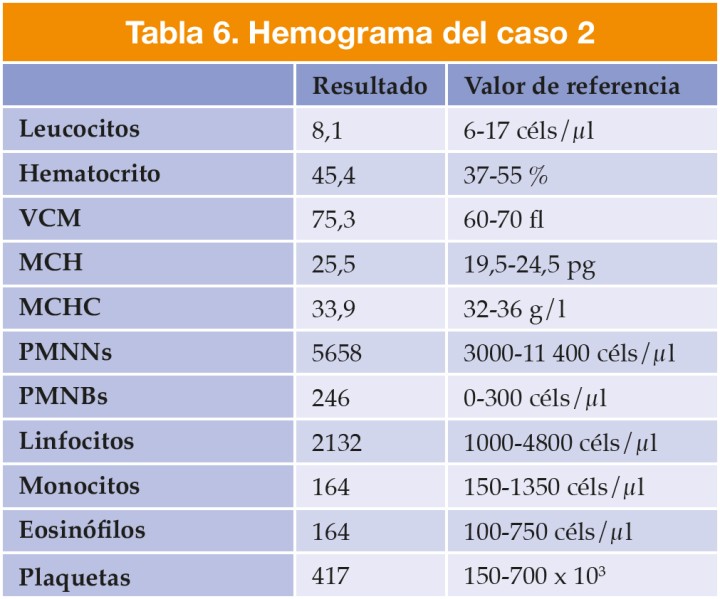
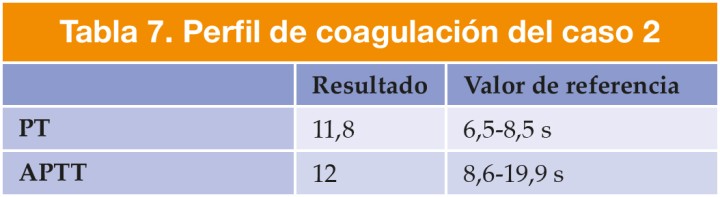
Se presentó en consulta una perra hembra no castrada de raza caniche, de 14 meses de edad y 4,8 kg de peso. Los resultados de la exploración general y la analítica inicial se muestran en las Tablas 5, 6 y 7.
VCM: volumen corpuscular medio; MCH: hemoglobina corpuscular media; MCHC: concentración de hemoglobina corpuscular media; PMNNs: neutrófilos polimorfonucleares; PMNBs: basófilos polimorfonucleares.
PT: tiempo de protrombina; APTT: tiempo parcial de tromboplastina activada.
Como tratamiento, en este caso se administró apomorfina (Emedog 1 mg/ml, Dômes Pharma, Pont-du-Château), 0,1 mg/kg de forma subcutánea, para inducir el vómito. La paciente vomitó contenido gástrico, sin observarse la presencia de restos de pastillas. Se administró también vitamina K1 endovenosa lenta (Vitamina K1 10 mg/ml, Dômes Pharma, Pont-du-Château), 5 mg/kg/12 horas. Se administró carbón activo con catártico (Carbodote Prime con carbón vegetal 30% y sulfato de sodio 6,25%, Dômes Pharma, Pont-du-Château), a dosis de 23,4 g, seguido de carbón activo solo (Carbodote Repeat con carbón vegetal 30%, Dômes Pharma, Pont-du-Château) a dosis de 21,6 g cada 6 horas vía oral.
La paciente no mostró síntomas relacionados con coagulopatía durante las horas que estuvo hospitalizada. Fue también dada de alta a las 24 horas con tratamiento de vitamina K1 a dosis de 1 mg/kg vía oral, cada 12 horas, durante 3 semanas y con recomendación de monitorizar el tiempo de protrombina a las 48 y a las 72 horas después de acabar el tratamiento.
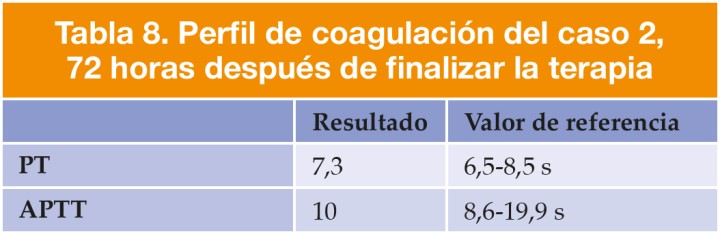
Los controles, realizados 72 horas después de finalizar el tratamiento con vitamina K1 (Tabla 8), dieron valores dentro de la normalidad. No se realizaron controles a las 48 horas de finalizado el mismo.
PT: tiempo de protrombina; APTT: tiempo parcial de tromboplastina activada.
¿Qué es el acenocumarol, cómo funciona y qué diferencia hay con los rodenticidas anticoagulantes?
El acenocumarol es un derivado de la cumarina que actúa como antagonista de la vitamina K. Inhibe la gammacarboxilación hepática de los factores de coagulación dependientes de la vitamina K en 3-5 horas (II, VII, IX, X). Esta gammacarboxilación tiene una relación significativa sobre la interacción de los factores de coagulación referidos con los iones calcio. Sin esta reacción, la coagulación sanguínea no puede iniciarse.1 Este producto inhibe la enzima vitamina K1 epóxido reductasa, que es la encargada de reconvertir la vitamina K1 epóxido en vitamina K1 activa de nuevo. Como consecuencia de esta inhibición, se van agotando las reservas de vitamina K1 y las de los factores de coagulación dependientes de la vitamina K1 que son elaborados en el hígado. Esto es común con los rodenticidas anticoagulantes, tanto de primera como de segunda generación. La diferencia se encuentra en el tiempo de actuación. En la intoxicación por rodenticidas anticoagulantes, la inhibición de la coagulación no será evidente hasta las 36-72 horas tras la ingesta, y las hemorragias aparecen a los 3-5 días tras la misma,2 mientras que con el acenocumarol, la inhibición de los factores de coagulación se da en 3-5 horas, por lo que podemos esperar signos de hemorragia más precoces.1
¿Qué importancia tiene hablar de este tipo de intoxicaciones?
Consideramos importante este caso clínico, dado que no se han descrito en la bibliografía casos anteriores de intoxicación aguda por acenocumarol en veterinaria. En humana, se describen casos de intoxicación por ingesta crónica o reacciones adversas;4,5 solo se describe un caso de intoxicación aguda en una niña por ingesta accidental que fue tratada y monitorizada del mismo modo que lo hacemos en veterinaria para los casos de ingesta de rodenticidas anticoagulantes.3
Dado que el mecanismo de acción del acenocumarol es igual al de los rodenticidas anticoagulantes, es vital ser conscientes de que cada vez con más frecuencia se pueden dar este tipo de accidentes y debemos estar preparados.
¿Cómo se diagnostica y se maneja este tipo de intoxicaciones comparado con el modo en que se manejaron estos casos?
En general, las dosis únicas (aunque elevadas) de acenocumarol no suelen ser peligrosas, pero la aparición y gravedad de los síntomas depende de la sensibilidad individual a los anticoagulantes orales, la cantidad ingerida y la duración del tratamiento.1
El signo principal es la hemorragia. En medicina humana, el 80 % de los casos presentan hemorragia cutánea, 52 % presentan hematomas, sangrado gastrointestinal, hematemesis, sangrado uterino, epistaxis, sangrado gingival y sangrado en las articulaciones.
En medicina humana se han descrito casos de hemoptisis en pacientes en tratamiento con acenocumarol que presentan otras comorbilidades como hipertensión, edad avanzada, presencia de hemorragias previas, insuficiencia renal, hepatopatía, anemia, uso de otros antiagregantes o uso de antiinflamatorios.1
También se han dado casos de vasculitis inmunomediada por IgA con afectación cutánea, articular y renal (hematuria y proteinuria). Se ha sugerido que este hecho se ve favorecido por la presencia de antígenos por infecciones de vías altas y también algunos fármacos. Los pacientes pueden sufrir de púrpura palpable, poliartralgias, glomerulonefritis leve y dolor abdominal.4
Al mismo tiempo, también se ha demostrado daño hepático asociado a la exposición de acenocumarol. Parece ser que hay una relación potencial entre el acenocumarol y la toxicidad hepática.5
La actividad anticoagulante del acenocumarol, al igual que la de los rodenticidas anticoagulantes, se mide utilizando el Tiempo de Protrombina (TP), afectando a la vía extrínseca de la cascada de la coagulación (factores VII, X, V y II implicados).1
En pacientes que han ingerido recientemente el anticoagulante está indicada la descontaminación por emesis siempre que el paciente no tenga otras comorbilidades que la contraindiquen (convulsiones, enfermedad cardiovascular significativa o procesos que reduzcan el estado de alerta). En el único caso de intoxicación accidental en personas (una bebé de 20 meses de edad), la paciente había vomitado antes de acudir al hospital y no plantearon la posibilidad de un lavado gástrico aunque hacía solamente una hora de la ingesta.3
En pacientes sintomáticos la estabilización es crítica. Puede ser necesario administrar oxígeno si presentan disnea, también transfusión de sangre entera o plasma fresco congelado para reponer sangre y factores de coagulación.2
Si el paciente ya está sangrando, la descontaminación no está indicada porque indica que la exposición puede haber ocurrido muchos días antes. El antídoto a utilizar es la vitamina K1. La vía de administración más adecuada es la vía oral, porque irá directa al hígado, donde se activarán los factores de coagulación a través de la circulación portal.2
Nosotros optamos por inducir el vómito y proceder, posteriormente, con el resto del tratamiento según hemos indicado (Tabla 9), iniciando la administración de carbón activado juntamente con un catártico, evitando así que los valores de anticoagulante aumentaran en sangre y facilitando su eliminación digestiva. Si no fuera posible la emesis o esta no fuera eficaz, se puede valorar empezar directamente con el carbón activado y el catártico, o realizar un lavado gástrico si el clínico lo viera necesario. Tras la primera administración de carbón activo, se pauta cada 4-6 horas durante un total de 24-48 horas. En pacientes asintomáticos, se puede optar tanto por iniciar tratamiento profiláctico con vitamina K1, como por monitorizar el valor de PT (tiempo de protrombina) y solamente iniciar la vitamina K1 si el PT está elevado. Si se optase por esta segunda opción, se recoge un valor basal y se repite a las 48 y 72 horas tras la exposición. El valor basal es importante porque sirve para determinar si ha habido exposiciones previas sin conocimiento del tutor. No se necesitará tratamiento con antídoto si la PT se mantiene normal a las 72 horas de la exposición. Sin embargo, cualquier elevación en la PT sería indicativo para comenzar el tratamiento completo con vitamina K1 (5 mg/kg/24 horas por vía oral junto a una comida un poco grasienta para mejorar su absorción). La recomendación más segura es mantener el tratamiento durante 21 días y repetir el PT a las 48-72 horas de interrumpir el tratamiento. Si los valores aún están elevados, continuar una semana más y repetir de nuevo la PT a las 48-72 horas de interrumpirlo de nuevo.6
Se deberá tener en cuenta que si hay que administrar medicaciones orales al mismo tiempo que el carbón activado, este puede interferir en su absorción y reducir su eficacia. Se recomienda dejar pasar unas 2 horas entre la administración del carbón y la medicación oral.8
Discusión
El uso de la vitamina K1 en medicina veterinaria es ampliamente conocido como el antídoto para el tratamiento de las intoxicaciones por raticidas cumarínicos.
Este tipo de intoxicación es una de las más frecuentes que se encuentran los centros veterinarios según una encuesta encargada por Dômes Pharma en España en el año 2022, realizada a 1000 veterinarios, y que coincide con los datos presentados por el Instituto Nacional de Toxicología y Ciencias Forenses en 2022,9 en el que los biocidas (38,1 %), grupo del que forman parte los raticidas, eran la mayor causa de intoxicación en animales.
La vitamina K1 revierte el efecto anticoagulante de las cumarinas; el contenido hepático de vitamina K1 tiene una correlación directa con la disminución del tiempo de protrombina. El acortamiento del tiempo de protrombina se puede apreciar en 4-8 horas tras la administración de la vitamina.10
Con este artículo queremos dar relevancia al hecho de que nuestras mascotas pueden verse igualmente afectadas por otra familia de cumarínicos que pueden ser falsamente considerados como menos nocivos, y son los que se utilizan en medicina humana para manejo de procesos tromboembólicos, entre otros.
Según los mismos datos presentados en 2022 por el Instituto Nacional de Toxicología y Ciencias Forenses, la segunda causa más frecuente de intoxicación en animales fue por medicamentos (25,8 %),9 de manera que aunque la ingestión de acenocumarol es menos frecuente que en el caso de raticidas cumarínicos en medicina veterinaria, sus efectos son igual de nocivos para los animales y su manejo es exactamente igual.
Es fundamental conocer que ante la ingesta accidental de fármacos como el acenocumarol (Sintrom® 4 mg), se debe proceder igual que frente a la ingesta de conocidos tóxicos que interfieren en el metabolismo de la vitamina K.
Aquí hemos descrito dos casos de ingesta accidental de acenocumarol y hemos ofrecido indicaciones de su manejo.
Fuente de financiación: artículo esponsorizado por Dômes Pharma.
Conflicto de intereses: la autora declara que este artículo es una colaboración con Dômes Pharma.
Bibliografía
- 1.
Ministerio de Sanidad, política social y de igualdad. Agencia española de medicamentos y productos sanitarios. Ficha técnica Sintrom comprimidos. AEMPS. CIMA. ES. FECHA DE LA REVISIÓN DEL TEXTO 06/2021.
- 2.
DeClementi C, Sobczak BR: Common Rodenticide Toxicoses in Small Animals. Vet Clin Small Anim 2018; 48: 1027-1038.
[PubMed] - 3.
Brands MR, Sytema J, van Hulst M, Kamps AWA: Unintentional ingestion of a high dose of acenocoumarol in a young child. BMJ Case Rep 2021;14:e240365.
[PubMed] - 4.
Esteban Terradillos S, Erdozain Castiella JG, Goiri Aparicio JM, et al.: Vasculitis IgA inducida por acenocumarol. Reumatol Clin. 2020;16(5):362-363.
[PubMed] - 5.
Gruz F, Anders M: Drug induced liver injury associated with acenocumarol exposure. Drugs & Therapy Perspectives 2021; 37(3): 120-123.
- 6.
Hovda LR, Brutlag AG, Poppenga RH, Peterson KL. Blackwell’s Five-Minute Veterinary Consult Clinical Companion: Small Animal Toxicology, Second Edition.. 2016 John Wiley & Sons, Inc.
- 7.
Plumb’s Veterinary Drug Handbook. Pocket — 7th edition. Adjunctive treatment for toxin ingestion using sorbitol with activated charcoal, Charcoal, activated, Vitamin K1. Plumb DC. 2011. Wiley-Blackwell, Ames, Iowa, USA. 1567 pp. ISBN: 9780-4709-5965-7.
- 8.
Bates N, Rawson-Harris P, Edwards N. Common questions in veterinary toxicology. J Small Anim Pract 2015; 56: 298-306.
[PubMed] - 9.
Alonso A. Consultas por intoxicaciones en animales. Instituto Nacional de Toxicología y Ciencias Forenses Servicio de Información Toxicológica. Memoria 2022. Pp 31-36. Madrid 2023.
- 10.
Coon, WW, Willis PW III: Some aspects of the pharmacology of oral anticoagulants. Clinical Pharmacology & Therapeutics 1970; 11(3): 312-336.
[PubMed]